- Was ist ein Atom?
- Wie ist ein Atom aufgebaut?
- Wie verbinden sich Atome?
- Teile eines Atoms
- Geschichte des Atoms
- Molekül
Wir erklären, was ein Atom ist und wie jeder seiner Teile aufgebaut ist. Auch seine Geschichte, Studien darüber und was ein Molekül ist.

Was ist ein Atom?
Die kleinste Einheit, aus der die Angelegenheit.
Das Wort Atom stammt aus dem Altgriechischen (Atom, "Ohne Teilung") und wurde von den ersten Philosophen geprägt, um Theorien über die Zusammensetzung der Dinge, d. h. die Elementarteilchen der Universum. Seitdem, mit dem Aufkommen der Atommodelle, die Art und Weise, sie sich vorzustellen, hat sich enorm verändert, da ein Atommodell im Laufe der Jahrhunderte das vorherige abgelöst hat, bis wir das erreicht haben, das wir heute verwenden.
Atome haben die Eigenschaften von Chemisches Element die sich zusammensetzen, und die Elemente wiederum werden nach ihrer geordnet und klassifiziert Ordnungszahlen, elektronische Konfiguration und chemische Eigenschaften in Periodensystem der Elemente.
Das gleiche chemische Element kann aus verschiedenen Atomen der gleichen Klasse bestehen, d. h. mit der gleichen Ordnungszahl (Anzahl von Protonen die jedes Atom im Element hat), obwohl ihre Atommassen unterschiedlich sind.
Zum Beispiel gibt es verschiedene Atome desselben Elements, die sich in ihrer Anzahl von unterscheiden Neutronen, und man nennt sie Isotope, ein repräsentativer Fall sind die Isotope des Elements Kohlenstoff (12C, 13C, 14C). Jedes Atom gehört also abhängig von seiner Protonenzahl zum gleichen chemischen Element oder nicht, also gehören Atome mit der gleichen Protonenzahl zum gleichen chemischen Element.
Wie ist ein Atom aufgebaut?
Atome bestehen aus einem Kern und einem oder mehreren Elektronen (die eine negative Ladung haben) um ihn herum. Der Kern besteht aus Teilchen, die Protonen und Neutronen genannt werden. Protonen sind positiv geladen und Neutronen sind neutral. Die Menge der Protonen und Neutronen wird Nukleonen genannt.
Protonen und Elektronen werden durch die elektromagnetische Kraft (die Wechselwirkung geladener Teilchen mit elektrischen und magnetischen Feldern) zueinander angezogen, während Protonen und Neutronen durch die Kernkraft (eine Kraft, die nur die Teilchen erfahren, aus denen die Atomkern).
Wie verbinden sich Atome?
Atome können sich miteinander verbinden, um zu bilden chemische Verbindungen, was passiert, wenn sie ihre Elektronen auf die eine oder andere Weise teilen. Chemische Bindungen können sein kovalent, ionisch Ja metallisch, die kovalente molekulare Verbindungen, ionische Netzwerke oder metallische Verbindungen hervorruft (obwohl es wichtig ist, klarzustellen, dass keine chemische Bindung absolut kovalent oder ionisch ist). Auf diese Weise können sich Atome zu bilden Moleküle einfach wie die Wasser, sowie zu bilden Makromoleküle komplex wie Protein, DNA Ja RNA.
Obwohl sich Atome durch die Anordnung ihrer Teilchen voneinander unterscheiden, gilt auch, dass alle Atome des gleichen Elements exakt gleich sind: die Wasserstoffatome im Sonne Sie sind die gleichen, aus denen unser Körper besteht, und die Kohlenstoffatome im Körper eines Hundes sind identisch mit denen, aus denen ein Diamant besteht. Der Unterschied liegt in der Art und Weise, wie sich die Atome zu den verschiedenen chemischen Verbindungen verbinden, aus denen die Organe und Organsysteme in der lebende Kreaturen, die in der Industrie, und all die Materie, aus der das Universum besteht.
Teile eines Atoms
Atome bestehen aus zwei wesentlichen Teilen:
- Der Nukleus. Ungefähr 99,94% der Masse eines Atoms sind im Kern konzentriert, wo die Protonen und Neutronen (die zusammen "Nukleonen" genannt werden) durch starke Kernkräfte verbunden sind, die verhindert, dass die Protonen sich gegenseitig abstoßen und die gleiche elektrische aufladen.
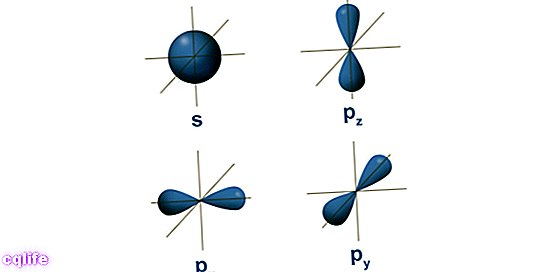
- Die Atomorbitale. Ein Orbital beschreibt einen Raumbereich, der den Atomkern umgibt, in dem die Wahrscheinlichkeit ein Elektron zu finden ist sehr hoch. Diese Bereiche haben unterschiedliche Formen, die durch das Lösen der stationären Schrödinger-Gleichung erhalten werden. Erwin Schrödinger war ein österreichischer Wissenschaftler, der 1925 diese Gleichung entwickelte, um die Entwicklung eines subatomaren Teilchens, wie beispielsweise Elektronen, zu berechnen. Damit bilden die Elektronen eine Art „Wolke“ um den Kern, die durch die Form der Atomorbitale dargestellt wird. Andererseits entspricht jedes Atomorbital einem bestimmten Energiewert für Elektronen, sodass sie nach ihren Energiewerten organisiert sind. Die folgende Abbildung zeigt die Formen der ersten Atomorbitale:
Geschichte des Atoms

Der erste, der die Idee der Existenz von Atomen formulierte, war der griechische Philosoph Demokrit (s.V-VI BC) aus rein imaginären Spekulationen (wie man die Wissenschaft damals verstanden hatte).
Seine Studien wurden von späteren Philosophen wie Leukippus und Epikur aufgegriffen, aber während der Zeit vernachlässigt mittelalterlich, überschattet von der kreationistischen Welterklärung, die alles Gott zuschrieb.
Wir mussten bis 1773 warten, als der französische Chemiker Antoine de Lavoisier seine Theorie über die Nichterschaffung oder Zerstörung von Materie (sie verwandelt sich nur) postulierte oder Gesetz der Erhaltung der Masse, die es John Dalton ermöglichte, 1804 die erste moderne Atomtheorie zu formulieren.
Aufeinanderfolgende Stipendiaten der körperlich und das Chemie Sie wurden von seiner Arbeit inspiriert, bessere und komplexere Systeme zum Verständnis der fundamentalen Teilchen der Materie vorzuschlagen. Anschließend wurden neue Atommodelle bis hin zu den heute am häufigsten verwendeten vorgeschlagen.
Die gegenwärtig akzeptierte Struktur ist diejenige, die aus der Experimente von Rutherford im Jahr 1911, zusammen mit den Formulierungen von Niels Bohr, Schrödinger und Heisenberg.
Molekül
Ein Molekül ist bekannt als die Vereinigung von zwei oder mehr Atomen durch chemische Bindungen, um eine komplexere und elektrisch neutralere Struktur zu bilden. Chemische Bindungen können kovalent oder ionisch sein.
Moleküle können aus Atomen desselben chemischen Elements bestehen, beispielsweise dem Sauerstoffmolekül (O2), oder aus Atomen verschiedener chemischer Elemente, beispielsweise dem Glucosemolekül. Als Moleküle gelten auch einatomige Gase, beispielsweise Helium (He).

